


ਕੈਂਸਰ ਦੇ ਜ਼ਿਆਦਾਤਰ ਰੂਪਾਂ ਲਈ ਬਿਮਾਰੀ ਦੇ ਪੜਾਅ (ਫੈਲਣ ਦੀ ਮਾਤਰਾ) ਦੀ ਪਛਾਣ ਕਰਨਾ ਮਹੱਤਵਪੂਰਨ ਹੈ। ਪ੍ਰਾਇਮਰੀ ਟਿਊਮਰ ਦਾ ਆਕਾਰ ਅਤੇ ਕੈਂਸਰ ਦੇ ਫੈਲਣ ਦੀ ਹੱਦ ਪੜਾਅ ਨੂੰ ਨਿਰਧਾਰਤ ਕਰਦੀ ਹੈ। ਇਹ ਇੱਕ ਵਿਅਕਤੀ ਦੇ ਪੂਰਵ-ਅਨੁਮਾਨ ਅਤੇ ਇਲਾਜ ਦੇ ਵਿਕਲਪਾਂ ਨੂੰ ਨਿਰਧਾਰਤ ਕਰਨ ਵਿੱਚ ਸਹਾਇਤਾ ਕਰ ਸਕਦਾ ਹੈ।
ਤੀਬਰ ਮਾਈਲੋਇਡ ਲਿਊਕੇਮੀਆ (ਏਐਮਐਲ), ਦੂਜੇ ਪਾਸੇ, ਬਹੁਤ ਘੱਟ ਨਤੀਜੇ ਵਜੋਂ ਟਿਊਮਰ ਬਣਦੇ ਹਨ। ਇਹ ਦੂਜੇ ਅੰਗਾਂ, ਜਿਵੇਂ ਕਿ ਜਿਗਰ ਅਤੇ ਤਿੱਲੀ ਵਿੱਚ ਫੈਲ ਗਿਆ ਹੈ, ਅਤੇ ਆਮ ਤੌਰ 'ਤੇ ਬੋਨ ਮੈਰੋ ਵਿੱਚ ਪ੍ਰਚਲਿਤ ਹੁੰਦਾ ਹੈ। ਨਤੀਜੇ ਵਜੋਂ, ਜ਼ਿਆਦਾਤਰ ਹੋਰ ਖ਼ਤਰਨਾਕ ਬਿਮਾਰੀਆਂ ਦੇ ਉਲਟ, AML ਸਟੇਜ ਨਹੀਂ ਕੀਤਾ ਜਾਂਦਾ ਹੈ। AML ਵਾਲੇ ਕਿਸੇ ਵਿਅਕਤੀ ਲਈ ਪੂਰਵ-ਅਨੁਮਾਨ ਵੱਖ-ਵੱਖ ਕਾਰਕਾਂ ਦੁਆਰਾ ਪ੍ਰਭਾਵਿਤ ਹੁੰਦਾ ਹੈ ਜਿਵੇਂ ਕਿ ਮਰੀਜ਼ ਦੀ ਉਮਰ, AML ਦਾ ਉਪ-ਕਿਸਮ (ਲੈਬ ਟੈਸਟਾਂ ਦੁਆਰਾ ਪਛਾਣਿਆ ਜਾਂਦਾ ਹੈ), ਅਤੇ ਵਾਧੂ ਲੈਬ ਟੈਸਟਾਂ ਦੇ ਨਤੀਜੇ।
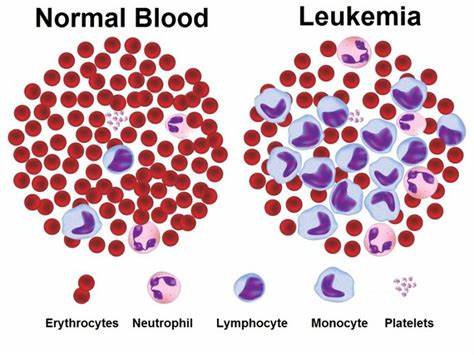
AML ਦੀਆਂ ਉਪ-ਕਿਸਮਾਂ ਨੂੰ ਕਈ ਤਰੀਕਿਆਂ ਨਾਲ ਵਰਗੀਕ੍ਰਿਤ ਕੀਤਾ ਜਾ ਸਕਦਾ ਹੈ। ਇਸ ਤੱਥ ਦੇ ਬਾਵਜੂਦ ਕਿ ਸਾਰੀਆਂ ਉਪ ਕਿਸਮਾਂ ਆਮ ਖੂਨ ਦੇ ਸੈੱਲਾਂ ਦੀ ਗਿਣਤੀ ਵਿੱਚ ਕਮੀ ਪੈਦਾ ਕਰਦੀਆਂ ਹਨ, AML ਦੇ ਵੱਖ-ਵੱਖ ਰੂਪ ਵੱਖੋ-ਵੱਖਰੇ ਲੱਛਣਾਂ ਅਤੇ ਮੁੱਦਿਆਂ ਨਾਲ ਜੁੜੇ ਹੋਏ ਹਨ। ਇਸ ਤੋਂ ਇਲਾਵਾ, ਹਰੇਕ ਉਪ-ਕਿਸਮ ਇੱਕ ਵਿਲੱਖਣ ਤਰੀਕੇ ਨਾਲ ਥੈਰੇਪੀ ਦਾ ਜਵਾਬ ਦੇ ਸਕਦੀ ਹੈ।
ਤੀਬਰ ਮਾਈਲੋਇਡ ਲਿਊਕੇਮੀਆ ਦਾ ਰੂਪ ਵਿਗਿਆਨ, ਜਾਂ ਮਾਈਕ੍ਰੋਸਕੋਪ ਦੇ ਹੇਠਾਂ ਘਾਤਕ ਸੈੱਲ ਕਿਵੇਂ ਦਿਖਾਈ ਦਿੰਦੇ ਹਨ, ਪਛਾਣ ਕੀਤੀ ਜਾਣ ਵਾਲੀ ਪਹਿਲੀ ਵਿਸ਼ੇਸ਼ਤਾ ਹੈ। AML ਨੂੰ ਇਸ ਅਧਾਰ 'ਤੇ ਸ਼੍ਰੇਣੀਬੱਧ ਕੀਤਾ ਗਿਆ ਹੈ ਕਿ ਇਹ ਇੱਕ ਆਮ, ਅਪੰਗ ਚਿੱਟੇ ਲਹੂ ਦੇ ਸੈੱਲ ਨਾਲ ਕਿੰਨੀ ਨਜ਼ਦੀਕੀ ਸਮਾਨ ਹੈ। AML ਵਾਲੇ ਜ਼ਿਆਦਾਤਰ ਮਰੀਜ਼ਾਂ ਵਿੱਚ ਮਾਈਲੋਇਡ ਲਿਊਕੇਮੀਆ ਵਜੋਂ ਜਾਣਿਆ ਜਾਂਦਾ ਇੱਕ ਉਪ-ਕਿਸਮ ਹੁੰਦਾ ਹੈ, ਜਿਸਦਾ ਮਤਲਬ ਹੈ ਕਿ ਬਿਮਾਰੀ ਨਿਊਟ੍ਰੋਫਿਲਜ਼ ਪੈਦਾ ਕਰਨ ਵਾਲੇ ਸੈੱਲਾਂ ਵਿੱਚ ਰਹਿੰਦੀ ਹੈ। ਮੋਨੋਬਲਾਸਟਿਕ ਜਾਂ ਮੋਨੋਸਾਈਟਿਕ ਲਿਊਕੇਮੀਆ ਏਐਮਐਲ ਦਾ ਇੱਕ ਰੂਪ ਹੈ ਜੋ ਦੂਜਿਆਂ ਨੂੰ ਪ੍ਰਭਾਵਿਤ ਕਰਦਾ ਹੈ। ਮੋਨੋਸਾਈਟਿਕ ਲਿਊਕੇਮੀਆ ਦੇ ਸੈੱਲ ਮੋਨੋਸਾਈਟਸ ਵਾਂਗ ਦਿਖਾਈ ਦਿੰਦੇ ਹਨ, ਜੋ ਕਿ ਚਿੱਟੇ ਖੂਨ ਦੇ ਸੈੱਲ ਹੁੰਦੇ ਹਨ। ਮਾਈਲੋਬਲਾਸਟਿਕ ਅਤੇ ਮੋਨੋਸਾਈਟਿਕ ਸੈੱਲ ਇਕੱਠੇ ਮਿਲ ਕੇ ਲਿਊਕੀਮੀਆ ਸੈੱਲ ਬਣ ਸਕਦੇ ਹਨ। AML ਉਹਨਾਂ ਸੈੱਲਾਂ ਦੇ ਕਾਰਨ ਜਾਪਦਾ ਹੈ ਜੋ erythroid ਜਾਂ megakaryocytic ਪਲੇਟਲੇਟ ਪੈਦਾ ਕਰਦੇ ਹਨ, ਜਾਂ ਸੈੱਲ ਜੋ ਲਾਲ ਖੂਨ ਦੇ ਸੈੱਲ ਬਣਾਉਂਦੇ ਹਨ।
ਤੀਬਰ ਮਾਈਲੋਇਡ ਲਿਊਕੇਮੀਆ ਦੇ ਉਪ-ਕਿਸਮ ਨੂੰ ਜਾਣਨਾ ਮਹੱਤਵਪੂਰਨ ਹੈ ਕਿਉਂਕਿ ਇਹ ਮਰੀਜ਼ ਦੇ ਪੂਰਵ-ਅਨੁਮਾਨ ਦੇ ਨਾਲ-ਨਾਲ ਸਭ ਤੋਂ ਵਧੀਆ ਥੈਰੇਪੀ ਵਿਕਲਪਾਂ ਨੂੰ ਪ੍ਰਭਾਵਤ ਕਰ ਸਕਦਾ ਹੈ। ਉਦਾਹਰਨ ਲਈ, ਤੀਬਰ ਪ੍ਰੋਮਾਈਲੋਸਾਈਟਿਕ ਲਿਊਕੇਮੀਆ (APL) ਉਪ-ਕਿਸਮ ਦਾ ਅਕਸਰ ਦਵਾਈਆਂ ਨਾਲ ਇਲਾਜ ਕੀਤਾ ਜਾਂਦਾ ਹੈ ਜੋ ਹੋਰ AML ਉਪ-ਕਿਸਮਾਂ ਲਈ ਨਹੀਂ ਵਰਤੀਆਂ ਜਾਂਦੀਆਂ ਹਨ। ਜੇਕਰ ਤੁਸੀਂ ਨਿਸ਼ਚਤ ਨਹੀਂ ਹੋ ਕਿ ਤੁਹਾਨੂੰ Acute myeloid leukemia ਦੀ ਕਿਹੜੀ ਉਪ ਕਿਸਮ ਹੈ, ਤਾਂ ਇਸ ਬਾਰੇ ਆਪਣੇ ਡਾਕਟਰ ਨਾਲ ਗੱਲ ਕਰੋ ਅਤੇ ਇਹ ਤੁਹਾਡੇ ਇਲਾਜ ਦੇ ਵਿਕਲਪਾਂ ਨੂੰ ਕਿਵੇਂ ਪ੍ਰਭਾਵਿਤ ਕਰ ਸਕਦਾ ਹੈ।
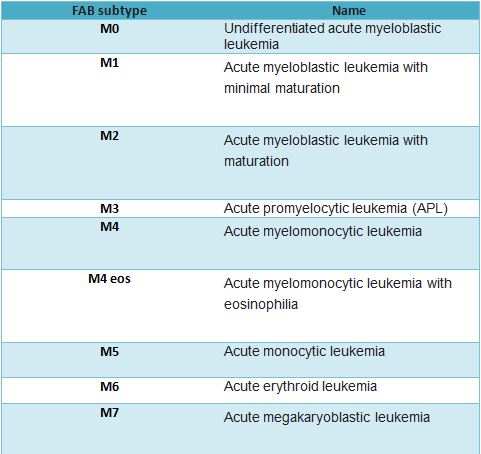
ਫ੍ਰੈਂਚ-ਅਮਰੀਕਨ-ਬ੍ਰਿਟਿਸ਼ (FAB) ਵਰਗੀਕਰਣ ਅਤੇ ਅੱਪਡੇਟ ਕੀਤਾ ਵਿਸ਼ਵ ਸਿਹਤ ਸੰਗਠਨ (WHO) ਵਰਗੀਕਰਣ ਏ.ਐੱਮ.ਐੱਲ. ਨੂੰ ਉਪ-ਕਿਸਮਾਂ ਵਿੱਚ ਵੰਡਣ ਲਈ ਸਭ ਤੋਂ ਵੱਧ ਵਰਤੇ ਜਾਣ ਵਾਲੇ ਦੋ ਵਰਗੀਕਰਨ ਹਨ।
| ਸ. ਨੰ. | FAB ਉਪ-ਕਿਸਮਾਂ | ਨਾਮ |
| 1. | M0 | ਅਵਿਭਾਗਿਤ ਤੀਬਰ ਮਾਈਲੋਬਲਾਸਟਿਕ ਲਿਊਕੇਮੀਆ |
| 2. | M1 | ਘੱਟ ਪਰਿਪੱਕਤਾ ਦੇ ਨਾਲ ਤੀਬਰ ਮਾਈਲੋਬਲਾਸਟਿਕ ਲਿਊਕੇਮੀਆ |
| 3. | M2 | ਪਰਿਪੱਕਤਾ ਦੇ ਨਾਲ ਤੀਬਰ ਮਾਈਲੋਬਲਾਸਟਿਕ ਲਿਊਕੇਮੀਆ |
| 4. | M3 | ਤੀਬਰ ਪ੍ਰੋਮੋਇਲੋਸਾਈਟਾਈਟਿਕ ਲਿuਕੇਮੀਆ (ਏਪੀਐਲ) |
| 5. | M4 | ਤੀਬਰ ਮਾਈਲੋਮੋਨੋਸਾਈਟਿਕ ਲੂਕਿਮੀਆ |
| 6. | M4 ਈਓਐਸ | ਈਓਸਿਨੋਫਿਲਿਆ ਦੇ ਨਾਲ ਤੀਬਰ ਮਾਈਲੋਮੋਨੋਸਾਈਟਿਕ ਲਿਊਕੇਮੀਆ |
| 7. | M5 | ਤੀਬਰ ਮੋਨੋਸਾਈਟਿਕ ਲਿਊਕੇਮੀਆ |
| 8. | M6 | ਤੀਬਰ erythroid leukemia |
| 9. | M7 | ਗੰਭੀਰ megakaryoblastic leukemia |
ਵਿਸ਼ਵ ਸਿਹਤ ਸੰਗਠਨ (WHO) ਦੁਆਰਾ AML ਦਾ ਵਰਗੀਕਰਨ ਇਸ ਪ੍ਰਕਾਰ ਹੈ:
ਹਾਲਾਂਕਿ FAB ਵਰਗੀਕਰਨ ਪ੍ਰਣਾਲੀ ਲਾਭਦਾਇਕ ਹੈ, ਇਹ ਉਹਨਾਂ ਬਹੁਤ ਸਾਰੇ ਵੇਰੀਏਬਲਾਂ ਨੂੰ ਨਜ਼ਰਅੰਦਾਜ਼ ਕਰਦੀ ਹੈ ਜੋ ਹੁਣ ਪੂਰਵ-ਅਨੁਮਾਨ (ਆਊਟਲੁੱਕ) ਨੂੰ ਪ੍ਰਭਾਵਿਤ ਕਰਨ ਲਈ ਜਾਣੇ ਜਾਂਦੇ ਹਨ। ਇਹਨਾਂ ਵਿੱਚੋਂ ਕੁਝ ਵਿਸ਼ੇਸ਼ਤਾਵਾਂ ਨੂੰ ਵਿਸ਼ਵ ਸਿਹਤ ਸੰਗਠਨ (WHO) ਵਰਗੀਕਰਣ ਵਿੱਚ ਸ਼ਾਮਲ ਕੀਤਾ ਗਿਆ ਹੈ, ਜੋ ਕਿ AML ਨੂੰ ਸਹੀ ਢੰਗ ਨਾਲ ਪਰਿਭਾਸ਼ਿਤ ਕਰਨ ਦੀ ਕੋਸ਼ਿਸ਼ ਵਿੱਚ 2016 ਵਿੱਚ ਸਭ ਤੋਂ ਹਾਲ ਹੀ ਵਿੱਚ ਸੋਧਿਆ ਗਿਆ ਸੀ।
WHO AML ਨੂੰ ਕਈ ਸ਼੍ਰੇਣੀਆਂ ਵਿੱਚ ਸ਼੍ਰੇਣੀਬੱਧ ਕਰਦਾ ਹੈ: AML ਵਿੱਚ ਕੁਝ ਜੈਨੇਟਿਕ ਵਿਗਾੜ (ਜੀਨ ਜਾਂ ਕ੍ਰੋਮੋਸੋਮ ਤਬਦੀਲੀਆਂ)
ਮਾਈਲੋਡੀਸਪਲੇਸੀਆ ਦੇ ਕਾਰਨ ਏਐਮਐਲ ਵਿੱਚ ਤਬਦੀਲੀਆਂ
AML ਕਾਰਨ ਹੋਇਆ ਕੀਮੋਥੈਰੇਪੀ ਜਾਂ ਅਤੀਤ ਵਿੱਚ ਰੇਡੀਏਸ਼ਨ ਇਲਾਜ
ਜੇਕਰ ਤੀਬਰ ਮਾਈਲੋਇਡ ਲਿਊਕੇਮੀਆ ਦਾ ਜ਼ਿਕਰ ਨਹੀਂ ਕੀਤਾ ਗਿਆ ਹੈ (ਇਹ FAB ਵਰਗੀਕਰਨ ਨਾਲ ਤੁਲਨਾਯੋਗ ਹੈ ਅਤੇ AML ਦੇ ਨਾਲ ਉਦਾਹਰਨਾਂ ਨੂੰ ਕਵਰ ਕਰਦਾ ਹੈ ਜੋ ਉਪਰੋਕਤ ਸ਼੍ਰੇਣੀਆਂ ਵਿੱਚੋਂ ਇੱਕ ਵਿੱਚ ਫਿੱਟ ਨਹੀਂ ਹੁੰਦੇ ਹਨ।)
ਅਵਿਭਾਗੀ ਅਤੇ ਬਾਈਫੇਨੋਟਾਈਪਿਕ ਤੀਬਰ ਲਿਊਕੇਮੀਆ ਲਿਊਕੇਮੀਆ ਹਨ ਜਿਨ੍ਹਾਂ ਵਿੱਚ ਲਿਮਫੋਸਾਈਟਿਕ ਅਤੇ ਮਾਈਲੋਇਡ ਵਿਸ਼ੇਸ਼ਤਾਵਾਂ ਦੋਵੇਂ ਹੁੰਦੀਆਂ ਹਨ ਪਰ ਸਿਰਫ਼ ਏਐਮਐਲ ਨਹੀਂ ਹੁੰਦੀਆਂ ਹਨ। ਮਿਕਸਡ ਫੀਨੋਟਾਈਪਾਂ ਵਾਲੇ ਤੀਬਰ ਲਿਊਕੇਮੀਆ ਨੂੰ ਮਿਕਸਡ ਫੀਨੋਟਾਈਪ ਐਕਿਊਟ ਲਿਊਕੇਮੀਆ (MPALs) ਵਜੋਂ ਵੀ ਜਾਣਿਆ ਜਾਂਦਾ ਹੈ।
ਸਾਈਟੋਜੈਨਿਕ:
ਲਿਊਕੇਮੀਆ ਸੈੱਲਾਂ ਵਿੱਚ ਪਛਾਣੇ ਗਏ ਸਾਇਟੋਜੇਨੇਟਿਕ (ਕ੍ਰੋਮੋਸੋਮ) ਤਬਦੀਲੀਆਂ ਨੂੰ ਵੀ ਬਿਮਾਰੀ ਦਾ ਵਰਗੀਕਰਨ ਕਰਨ ਲਈ ਵਰਤਿਆ ਜਾਂਦਾ ਹੈ। AML ਸੈੱਲਾਂ ਦੀ ਦਿੱਖ ਅਤੇ ਕੁਝ ਕ੍ਰੋਮੋਸੋਮਲ ਤਬਦੀਲੀਆਂ ਨੇੜਿਓਂ ਜੁੜੀਆਂ ਹੋਈਆਂ ਹਨ। ਵਧੇਰੇ ਮਹੱਤਵਪੂਰਨ ਤੌਰ 'ਤੇ, ਕ੍ਰੋਮੋਸੋਮਲ ਤਬਦੀਲੀਆਂ ਕਦੇ-ਕਦਾਈਂ ਇਹ ਸੰਕੇਤ ਦੇ ਸਕਦੀਆਂ ਹਨ ਕਿ ਤੀਬਰ ਇਲਾਜ ਕਿੰਨੀ ਚੰਗੀ ਤਰ੍ਹਾਂ ਕੰਮ ਕਰੇਗਾ, ਜੋ ਡਾਕਟਰਾਂ ਨੂੰ ਵਧੀਆ ਇਲਾਜ ਵਿਕਲਪਾਂ ਨੂੰ ਨਿਰਧਾਰਤ ਕਰਨ ਵਿੱਚ ਸਹਾਇਤਾ ਕਰਦਾ ਹੈ। ਇਹ ਸੰਭਾਵਨਾ ਕਿ ਥੈਰੇਪੀ AML ਦੇ ਉਪ-ਕਿਸਮ ਦੇ ਵਿਰੁੱਧ ਕੰਮ ਕਰੇਗੀ, ਖਾਸ ਤੌਰ 'ਤੇ ਕ੍ਰੋਮੋਸੋਮਲ ਅਸਧਾਰਨਤਾਵਾਂ ਦੁਆਰਾ ਸ਼੍ਰੇਣੀਬੱਧ ਕੀਤੀ ਜਾਂਦੀ ਹੈ।
1 ਤੋਂ 22 ਤੱਕ, ਸਾਰੇ ਕ੍ਰੋਮੋਸੋਮ ਨੰਬਰ ਕੀਤੇ ਜਾਂਦੇ ਹਨ। ਅੱਖਰ "p" ਅਤੇ "q" ਕ੍ਰੋਮੋਸੋਮ ਦੇ "ਬਾਹਾਂ" ਜਾਂ ਖਾਸ ਖੇਤਰਾਂ ਨਾਲ ਸਬੰਧਤ ਹਨ, ਜਦੋਂ ਕਿ "X" ਅਤੇ "Y" ਲਿੰਗ ਕ੍ਰੋਮੋਸੋਮ ਨੂੰ ਸੰਕੇਤ ਕਰਦੇ ਹਨ। AML ਕਈ ਤਰ੍ਹਾਂ ਦੇ ਜੈਨੇਟਿਕ ਤਬਦੀਲੀਆਂ ਨਾਲ ਜੁੜਿਆ ਹੋਇਆ ਹੈ, ਜਿਸ ਵਿੱਚ ਸ਼ਾਮਲ ਹਨ:
ਹੇਠਾਂ ਕੁਝ ਸਭ ਤੋਂ ਵੱਧ ਪ੍ਰਚਲਿਤ ਕ੍ਰੋਮੋਸੋਮਲ ਤਬਦੀਲੀਆਂ ਹਨ:
ਅਨੁਕੂਲ. ਬੈਂਡ p16 ਅਤੇ q13 [t(22;16)(p16;q13), inv(22)(p16q13)] ਵਿੱਚ ਕ੍ਰੋਮੋਸੋਮ 22 ਦੀਆਂ ਅਸਧਾਰਨਤਾਵਾਂ ਨੂੰ ਬਿਹਤਰ ਇਲਾਜ ਦੇ ਨਤੀਜਿਆਂ ਨਾਲ ਜੋੜਿਆ ਗਿਆ ਹੈ। ਅਤੇ ਕ੍ਰੋਮੋਸੋਮਸ 8 ਅਤੇ 21 ਵਿਚਕਾਰ ਇੱਕ ਟ੍ਰਾਂਸਲੋਕੇਸ਼ਨ [t(8;21)]।
ਸਧਾਰਣ ਕ੍ਰੋਮੋਸੋਮ ਬਿਨਾਂ ਕਿਸੇ ਬਦਲਾਅ ਦੇ ਅਤੇ ਕ੍ਰੋਮੋਸੋਮ 9 ਅਤੇ 11 [t(9;11)] ਦੇ ਵਿਚਕਾਰ ਇੱਕ ਟ੍ਰਾਂਸਲੋਕੇਸ਼ਨ ਇੱਕ ਖਰਾਬ ਪੂਰਵ-ਅਨੁਮਾਨ ਨਾਲ ਜੁੜੇ ਦੋ ਬਦਲਾਅ ਹਨ। ਬਹੁਤ ਸਾਰੀਆਂ ਵਾਧੂ ਉਪ-ਕਿਸਮਾਂ, ਖਾਸ ਤੌਰ 'ਤੇ ਇੱਕ ਜਾਂ ਵਧੇਰੇ ਵਿਲੱਖਣ ਅਣੂ ਤਬਦੀਲੀਆਂ ਵਾਲੇ, ਇਸ ਸ਼੍ਰੇਣੀ ਵਿੱਚ ਸ਼ਾਮਲ ਕੀਤੇ ਗਏ ਹਨ। ਕ੍ਰੋਮੋਸੋਮ 8 ਜਾਂ ਟ੍ਰਾਈਸੋਮੀ 8 ਦੀਆਂ ਵਾਧੂ ਕਾਪੀਆਂ ਨੂੰ ਕਈ ਵਾਰ ਅਣਉਚਿਤ ਜੋਖਮ (ਹੇਠਾਂ ਦੇਖੋ) ਦੇ ਮੁਕਾਬਲੇ ਵਿਚਕਾਰਲੇ ਜੋਖਮ ਵਜੋਂ ਸ਼੍ਰੇਣੀਬੱਧ ਕੀਤਾ ਜਾਂਦਾ ਹੈ।
ਪ੍ਰਤੀਕੂਲ: ਕ੍ਰੋਮੋਸੋਮ 8 ਜਾਂ 13 ਦੀਆਂ ਵਾਧੂ ਕਾਪੀਆਂ [ਉਦਾਹਰਨ ਲਈ, ਟ੍ਰਾਈਸੋਮੀ 8 (+8)], ਕ੍ਰੋਮੋਸੋਮ 5 ਜਾਂ 7 ਦੇ ਸਾਰੇ ਜਾਂ ਹਿੱਸੇ ਨੂੰ ਮਿਟਾਉਣਾ, ਮਲਟੀਪਲ ਕ੍ਰੋਮੋਸੋਮਜ਼ 'ਤੇ ਗੁੰਝਲਦਾਰ ਤਬਦੀਲੀਆਂ, ਅਤੇ ਬੈਂਡ q3 'ਤੇ ਕ੍ਰੋਮੋਸੋਮ 26 ਵਿੱਚ ਬਦਲਾਅ ਕ੍ਰੋਮੋਸੋਮ ਦੀਆਂ ਉਦਾਹਰਣਾਂ ਹਨ। ਘੱਟ ਪ੍ਰਭਾਵੀ ਥੈਰੇਪੀ ਜਾਂ AML ਨੂੰ ਠੀਕ ਕਰਨ ਦੀ ਮਾੜੀ ਸੰਭਾਵਨਾ ਨਾਲ ਜੁੜੀਆਂ ਤਬਦੀਲੀਆਂ।
ਆਮ ਤੌਰ 'ਤੇ, ਨੌਜਵਾਨ ਵਿਅਕਤੀਆਂ ਵਿੱਚ ਸਕਾਰਾਤਮਕ ਤਬਦੀਲੀਆਂ ਵਧੇਰੇ ਪ੍ਰਚਲਿਤ ਹੁੰਦੀਆਂ ਹਨ, ਜਦੋਂ ਕਿ 60 ਸਾਲ ਤੋਂ ਵੱਧ ਉਮਰ ਦੇ ਵਿਅਕਤੀਆਂ ਵਿੱਚ ਨਕਾਰਾਤਮਕ ਤਬਦੀਲੀਆਂ ਦੀ ਜ਼ਿਆਦਾ ਸੰਭਾਵਨਾ ਹੁੰਦੀ ਹੈ। ਇਹਨਾਂ ਸਮੂਹਾਂ ਵਿੱਚੋਂ ਹਰੇਕ ਵਿੱਚ, ਥੈਰੇਪੀ ਦੀ ਪ੍ਰਭਾਵਸ਼ੀਲਤਾ ਅਜੇ ਵੀ ਬਹੁਤ ਵੱਖਰੀ ਹੁੰਦੀ ਹੈ। ਅਨੁਕੂਲ AML ਵਾਲੇ 50 ਸਾਲ ਤੋਂ ਘੱਟ ਉਮਰ ਦੇ 60% ਤੋਂ 60% ਮਰੀਜ਼ਾਂ ਅਤੇ 10 ਸਾਲ ਤੋਂ ਘੱਟ ਉਮਰ ਦੇ 60% ਤੋਂ ਘੱਟ ਮਰੀਜ਼ਾਂ ਲਈ ਅਣਉਚਿਤ ਏ. 60 ਸਾਲ ਤੋਂ ਵੱਧ ਉਮਰ ਦੇ ਮਰੀਜ਼ਾਂ ਦਾ ਪੂਰਵ-ਅਨੁਮਾਨ ਕਾਫ਼ੀ ਮਾੜਾ ਹੁੰਦਾ ਹੈ। ਹੋਰ ਮਾਪਦੰਡ, ਜਿਵੇਂ ਕਿ ਚਿੱਟੇ ਰਕਤਾਣੂਆਂ ਦੀ ਗਿਣਤੀ, ਪ੍ਰਭਾਵੀ ਥੈਰੇਪੀ ਦੇ ਕੰਮ ਕਰਨ ਦੇ ਤਰੀਕੇ ਨੂੰ ਪ੍ਰਭਾਵਤ ਕਰਦੇ ਹਨ। ਇਹ ਨਿਸ਼ਚਤਤਾ ਨਾਲ ਜਾਣਨਾ ਅਸੰਭਵ ਹੈ ਕਿ ਕਿਸੇ ਵਿਅਕਤੀ ਦਾ ਇਲਾਜ ਕਿੰਨਾ ਪ੍ਰਭਾਵਸ਼ਾਲੀ ਹੋਵੇਗਾ।
ਰਿਸ਼ੀ ਕਪੂਰ ਦੀ ਘਟਨਾ:
ਇਹ ਦੇਸ਼ ਅਤੇ ਫਿਲਮ ਉਦਯੋਗ ਲਈ ਇੱਕ ਗੈਰ-ਦੋਸਤਾਨਾ ਹਾਲਾਤ ਬਣ ਕੇ ਖਤਮ ਹੋ ਰਿਹਾ ਹੈ। ਕੱਲ੍ਹ ਇਰਫਾਨ ਖਾਨ ਅਤੇ ਅੱਜ ਰਿਸ਼ੀ ਕੁਮਾਰ, ਦੋਵੇਂ ਇੱਕ ਸਮਾਨ ਦੁਸ਼ਮਣ ਦੇ ਦੁਆਲੇ ਕਿੱਕਰ ਹੋ ਗਏ ਹਨ। ਰਿਸ਼ੀ ਕਪੂਰ ਇੱਕ ਔਨ-ਸਕ੍ਰੀਨ ਪਾਤਰ ਸੀ ਜਿਸਨੇ ਆਪਣੇ ਕਰੀਅਰ ਵਿੱਚ ਮੇਰਾ ਨਾਮ ਜੋਕਰ ਵਿੱਚ ਡੈਬਿਊ ਕਰਨ ਲਈ ਸਰਵੋਤਮ ਬਾਲ ਕਲਾਕਾਰ ਲਈ ਰਾਸ਼ਟਰੀ ਫਿਲਮ ਅਵਾਰਡ ਦਿੱਤੇ ਜਾਣ ਤੋਂ ਲੈ ਕੇ ਲਾਈਫਟਾਈਮ ਅਚੀਵਮੈਂਟ ਜਿੱਤਣ ਤੱਕ ਕਈ ਸਨਮਾਨ ਪ੍ਰਾਪਤ ਕੀਤੇ ਸਨ।
ਹਿੰਦੀ ਫਿਲਮ ਉਦਯੋਗ ਲਈ ਉਸ ਵੱਲੋਂ ਕੀਤੀਆਂ ਗਈਆਂ ਆਲੋਚਨਾਤਮਕ ਪ੍ਰਤੀਬੱਧਤਾਵਾਂ ਲਈ ਪੁਰਸਕਾਰ। ਇੱਕ ਔਨ-ਸਕ੍ਰੀਨ ਪਾਤਰ ਜੋ ਆਪਣੇ ਗਲੈਮਰਸ ਕੈਰੀਅਰ ਲਈ ਜਾਣਿਆ ਜਾਂਦਾ ਸੀ, 67 ਸਾਲ ਦੀ ਉਮਰ ਵਿੱਚ ਐਕਿਊਟ ਮਾਈਲੋਇਡ ਲਿਊਕੇਮੀਆ ਵਿਰੁੱਧ ਲੜਾਈ ਹਾਰ ਗਿਆ।
ਇਸ ਬਾਰੇ ਹੋਰ ਜਾਣੋ
https://zenonco.io/cancer/rishi-kapoor-acute-myeloid-leukaemia/